
海南普利制药股份有限公司(以下简称“普利制药”或“公司”)全资子公司安徽普利药业有限公司于近日向美国食品药品监督管理局(以下简称“FDA”)顺利提交了替韦立马原料药药物主文件(DMF)。
基本情况
(一)产品名称:替韦立马(曾用名:特考韦瑞)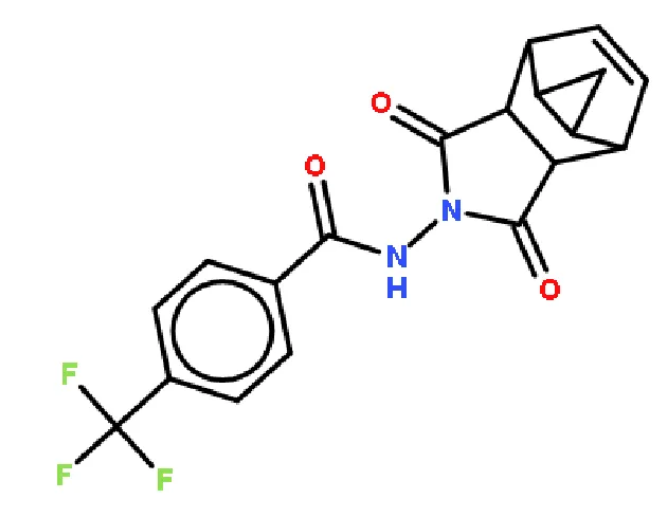
(二)剂型:原料药
(三)DMF号:038852
(四)包装规格:5kg/桶
(五)持有人:安徽普利药业有限公司
替韦立马(Tecovirimat)是一种小分子广谱膜蛋白抑制剂,通过抑制正痘病毒VP37蛋白的活性,阻止正痘蛋白形成病毒特异性包裹复合体,防止输出感染性包膜病毒粒,从而抑制病毒的细胞间传播和远程传播。替韦立马由Siga Technologies研发,2010年被FDA授予治疗痘病毒感染的孤儿药资格,并于2018年获批上市,用于成人和体重不小于13kg的儿童患者的天花病治疗,是首款获批的抗天花药物。2022年,欧洲药品管理局批准其用于治疗天花、猴痘、牛痘以及接种天花疫苗后的牛痘并发症。根据美国疾病预防控制中心(CDC)网站公布的信息,替韦立马已从2022年猴痘疾病爆发开始就以超说明书同情用药形式用于治疗猴痘病毒感染患者,在降低体内病毒数量上有积极作用。
2023年9月15日,国家卫健委公告,根据《中华人民共和国传染病防治法》相关规定,自2023年9月20日起将猴痘纳入乙类传染病进行管理,采取乙类传染病的预防、控制措施。国家疾控局、国家卫健委制定并印发的《猴痘防控方案》重点还是以预防为主,没有提到有效的抗病毒治疗方案。替韦立马目前国外已上市制剂包括注射剂、胶囊等,国内暂无制剂产品上市。
自猴痘疾病爆发以来,普利制药就前瞻性的对替韦立马原料和注射液启动了仿制研发工作,通过一年多的努力,目前进展如下:
替韦立马原料:已完成注册批的生产,并已向美国FDA提交了DMF文档(DMF号:038852),随后将向国家药品监督管理局药品审评中心提交原料药备案。替韦立马注射液:针对中、美双报工作正在抓紧进行中。
根据中国疾病预防控制中心2023年8月猴痘疾病监测情况:“2023年8月1日-31日,中国内地(不含港澳台)新增报告501例猴痘确诊病例”,“ 病例中有5例女性”。考虑到猴痘疾病将在我国一定时期内持续存在,并且传播速度加快,感染人群和情形更加复杂化,普利制药加急开发的替韦立马原料和注射液,在紧急情况下可为临时保障用药,将能为猴痘疾病的防控尽一份力量。
普利制药全资子公司安徽普利于今年完成了替韦立马原料药项目的建设并如期投产,日前提交美国DMF。公司将充分发挥全球注册和制造国际化优势,利用国际化的高端产能,助力猴痘治疗药物的研发,为全球猴痘疾病防控共同努力。
安徽普利药业是一家活性原料专业供应商,致力于向全球医药、保健和护肤领域提供化学合成、生物合成的高品质的特色原料和服务。
